沸騰(ふっとう、英語: boiling)とは、液体から気体へ相転移する気化が、液体の表面からだけでなく内部からも激しく起こる現象である。つまり水の場合で言えば、水の内部から水の分子が出て行くこととも言える。液体の内部からの気化を沸騰というのに対して、液体の表面で起こる気化は蒸発という。
概要
液体の蒸気圧は温度の上昇と共に増加する。蒸気圧が外圧(液体の表面にかかる圧力)と等しくなると、液体内部に気泡が発生し沸騰が起こる。このときの温度を沸点という。外圧がちょうど 1 気圧のときの沸点を標準沸点という。
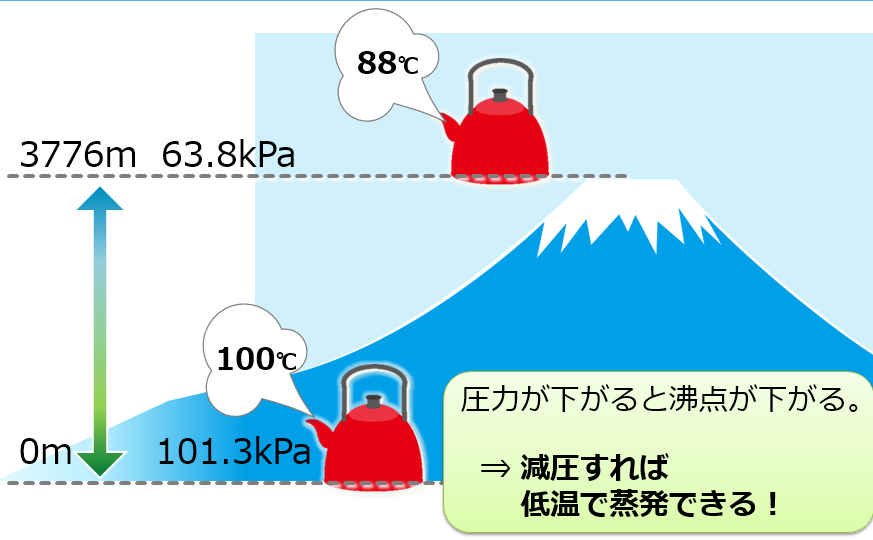
沸点は外圧(気圧)により変わる。外圧が 1 気圧より高くなると沸点は上昇し、低くなると降下する。例えば水は 1 気圧下では約 100 °C(正確には99.974 °C)で沸点に達するが、気圧の低い富士山頂では約 90 °Cで沸騰する。この原理は圧力鍋での調理、火力発電や原子力発電などにおいて応用されている。
不揮発性の物質(気体になりにくい物質)を液体に溶解させると沸点が上昇する。これは沸点上昇と呼ばれる。
突沸
沸点に達しているにもかかわらず相転移が生じず沸騰しないことがあり、この状態を過加熱という。この過加熱の状態の液体に振動などの刺激を与えると突発的な沸騰を起こすことがあり、これを突沸(とっぷつ)という。この突沸を防ぐため科学実験では沸騰石と呼ばれる多孔質の石が用いられる。また、電子レンジ、ガスコンロ、IHクッキングヒーター等を用いた調理過程でも突沸が起きることがあり、ただの水に限らず、豆乳やコーヒー、みそ汁やカレーなどを温めて容器に触れたりかき混ぜたり、調味料等を加えたわずかな刺激などで高温の液体が激しく弾けるように飛び散り火傷を負う事がある。そのため事故防止の観点から、急な加熱を避けるなどの注意喚起が行われている。
沸騰水
沸騰している水を沸騰水という。外圧が変化すると沸点も変わるが、通常は大気圧下で沸騰している約 100 °Cの水が沸騰水として実験で使用される。
常温の水に比べると、やや反応性が高い。たとえば、マグネシウムは、常温では水と反応しないが、沸騰水とは反応する。また、塩化鉄(III)水溶液は沸騰水によって加水分解が促進され、水酸化鉄(III)のコロイドと塩化物イオンと水素イオンに分解される。
沸騰の様相
沸騰には核沸騰と膜沸騰がある(沸騰曲線も参照)。
表現
「沸騰」は本来は水流が激しく泡立ち吹き上がる様な状態を指す熟語である。
また、水が沸騰する様から転じて、個人・集団や場の雰囲気が最高潮に盛り上がる様や不満が爆発する様も指す。
出典
参考文献
- 竹内敬人『化学の基礎』岩波書店、1996年。ISBN 4-00-007981-6。
関連項目
- 気化 - 沸点 - 気化熱
- 融解 - 融点 - 融解熱
- 凝固 - 凝固点
- 昇華
- 凝縮
- 臨界点
- 相 - 液体 - 固体 - 気体 - 蒸気
- 沸騰曲線
- パーコレーション
- 茹でる
- 炭酸ガス
- 乾燥
外部リンク
- 『沸騰』 - コトバンク